La insulina: una molécula milagrosa
Agustín López Munguía
Hay moléculas que podrían emplearse para describir el curso de la civilización humana: el agua pura, el azúcar de caña, la sal, o más recientemente la aspirina, o la penicilina. La ingeniería genética, herramienta cuyo desarrollo celebramos en este número, irrumpió en el mundo moderno aportando una de esas moléculas que caracterizan esta era: la insulina (Figura 1).
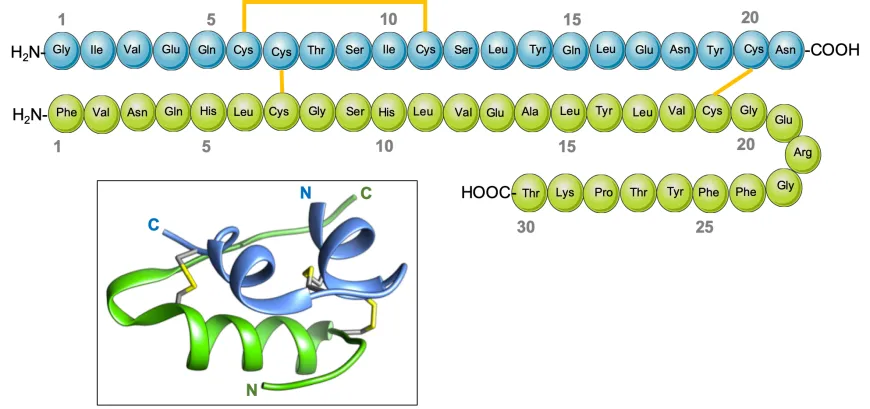
Figura 1. Estructura de la insulina. Contiene dos cadenas polipeptídicas, la Cadena A (azul) con 21 aminoácidos y la cadena B (verde) con 30 aminoácidos. Las conectan dos puentes de azufre, y existe uno más dentro de la cadena A. En la insulina porcina solo cambia los aminoácidos, Treonina en B30 por Alanina, mientras que en la insulina bovina cambian además la Treonina en A8 por Alanina y la Isoleucina 10 por Valina (Modificado de Prabu et al., 2023).
Biotecnología moderna, bioseguridad y los orígenes terapéuticos de la diabetes
El 29 de octubre de 2022 se cumplieron 40 años de un nuevo parteaguas en la historia de la biotecnología que abrió paso a la biotecnología moderna: la aprobación por parte de la FDA (la Food and Drug Administration en los EUA) de la insulina humana producida por una bacteria modificada genéticamente a través de técnicas de ADN recombinante para el tratamiento de la diabetes. La aprobación, que fue dada a conocer en la primera plana de los periódicos como el New York Times (Figura 2), solo tomó 5 meses. Henry Miller, director fundador de la Oficina para Biotecnología de la FDA, reseña esta historia en una publicación reciente (1). Destaca la decisión de que no se requería de nuevos paradigmas regulatorios para evaluar a la insulina recombinante, al considerar que la tecnología del ADN recombinante era solo una extensión o refinamiento de métodos tradicionales de producción de medicamentos por microorganismos.

Figura 2. Primera plana del New York Times del 30 de octubre de 1982, dando a conocer la aprobación de la FDA de la insulina humana producida por una bacteria modificada genéticamente para el tratamiento de la diabetes.
En 1922, 60 años antes de la aprobación de la insulina por la FDA se otorgó el Premio Nobel de Fisiología y Medicina a Frederick Grant Banting y a John James Richard Macleod. Ese mismo año, Banting y Charles Best lograron producir insulina de cerdo cruda a partir del páncreas, en realidad de restos de cerdos y vacas provenientes de la industria empacadora de carne, dando inicio al tratamiento terapéutico de la diabetes (Figura 3). Este acontecimiento lo evoca Martin Scorsese en la película “Los Asesinos de la Luna”, (Killers of the Flower Moon) de reciente estreno, cuando diabéticos de la tribu Osage al noreste de Oklahoma de pronto disponen de insulina.
Como suele suceder, hubo numerosas protestas de otros científicos que reclamaban ser incluidos en el reconocimiento, incluido el propio Charles Best, también ignorado por los jurados suecos (2).

Figura 3. (a) Los páncreas son examinados a su llegada a la planta procedentes del rastro, para posteriormente ser molidos (b), en el proceso desarrollado por Elli Lilly &Co. En la última etapa, el producto era filtrado y envasado (c y d). Fuente: Museo Nacional de Historia Estadounidense.
Al margen de la disputa por los honores, el trabajo de búsqueda/concentración/purificación de Banting y Best fue espectacular: de acuerdo con información publicada en el Blog del National Museum of American History (3), se requería de poco más de una tonelada de residuos de cerdos para obtener alrededor de 100g de insulina pura de puerco (Figura 4). De continuar esta tendencia, los 778 millones de cerdos que se producen al año en el mundo actualmente (58% en China), no hubieran alcanzado para tratar a los 570 millones de diabéticos.

Figura 4. Del páncreas del cerdo a la jeringa: muestras de las 4 etapas en el proceso de purificación del proceso de Elli Lilly en los años 40, de acuerdo con una publicación en el Blog del Museo Nacional de Historia (US). El producto en su forma más pura se obtenía a partir del vial 4.
Hoy la industria de medicamentos obtenidos por ingeniería genética es el sector económicamente más importante de la Industria farmacéutica. De acuerdo con el portal Drug Discovery and Devlopment (4), dentro de los 50 medicamentos con ventas por arriba de los dos mil millones de dólares en 2022, los cinco primeros son productos recombinantes o transgénicos, con la vacuna contra Covid-19 de Pfizer/BioNTech Comirnaty con ventas de casi 56 mil millones de dólares a la cabeza. En un redituable lugar número 49 en ventas se encuentra la insulina de acción prolongada (Lantus), producida por Sanofi, con ventas de 2 mil 343 millones de dólares. Si bien se enlistan por valor en el mercado, sería fantástico poder priorizarlas diseñando un índice que cuantificara y mostrara a la sociedad las vidas salvadas, el sufrimiento evitado o la calidad de vida ganada. Como sea, estos datos son evidencia concreta no solo del gran impacto de la Biotecnología Moderna en la sociedad, sino también de la seguridad de sus productos y vigilancia a la que han estado sujetos.
El IBt, la UNAM y la Biotecnología Moderna
La puerta que la ingeniería genética representa para que productos de genes de cualquier origen accedan a las farmacias primero y a las despensas posteriormente, vía su expresión en la bacteria Escherichia coli, se abre en la Universidad de California en San Francisco (UCSF) con los trabajos de Stanley Cohen, Herbert Boyer y colaboradores (5) y posteriormente de Goeddel y colaboradores (6) y de Francisco Bolívar, también con Herbert Boyer, y otros colaboradores (7) a través de la construcción de verdaderos vehículos moleculares, concretamente, plásmidos que entran a la célula hospedera, transportando genes de cualquier tipo de célula.
De hecho, el trabajo de Francisco Bolívar que describe el plásmido pBR322, un vehículo de clonación multipropósito, constituye el pilar sobre el que se sientan las bases de cientos de proyectos en el mundo para la producción de proteínas recombinantes en E. coli, estableciendo así los inicios de la ingeniería genética (figura 5). El trabajo del Dr. Bolívar ha sido citado en el Web of Science en 5 mil 347 ocasiones, siendo hasta la fecha una herramientas de trabajo de laboratorios de biología molecular. Se trató también de un parteaguas en la relación academia-industria, así como de la creación de empresas surgidas desde la academia. Es el caso de Genentech esencialmente creada por científicos, haciendo posible proyectos de investigación aplicada que iniciaron con la clonación del gen de la insulina. De acuerdo con Stephen Hall en el libro Invisible Frontiers (8), una vez abierta la opción de la ingeniería genética, se inicia una férrea competencia por lograr la producción de insulina humana por ingeniería genética.

Figura 5. Esquema de las dos principales estrategias de ingeniería genética seguidas por los grupos que participaron en la búsqueda del proceso para la síntesis de insulina (ver figura 4). A la izquierda la síntesis independiente de las cadenas A y B que la constituyen y su posterior ensamblaje; a la derecha, la síntesis de un precursor (preproinsulina) que contiene a la insulina integrada, ambas estrategias empleando el plásmido pBR3222 como vehículo molecular para transformar E.coli.
Parte de esta competencia fue también descrita recientemente por Arthur Riggs (9), integrante del llamado Somatostatin Team (Figura 6). Este grupo se integró para intentar, antes que la insulina, clonar el gen de la hormona humana somatostatina, convencidos por Riggs de que, aunque sin potencial de mercado, al ser mucho más pequeña y menos compleja (una sola cadena de 14 aminoácidos), el éxito demostraría a los inversionistas la viabilidad de la tecnología; lo que hoy llamamos la prueba de concepto. El proyecto le había sido rechazado por los Institutos Nacionales de Salud (NIH por sus siglas en inglés), calificándolo de tan solo un “ejercicio académico” sin mérito práctico. La expresión en E.coli de un gen sintetizado químicamente para producir somastotina fue así el primer éxito de la Ingeniería genética (10).

Figura 6. Científicos involucrados en el proyecto de la somatostatina en City of Hope, alrededor de 1977. En la foto, de izquierda a derecha: fila de atrás: Arthur Riggs, Herbert Boyer, Keiichi Itakura, Roberto Crea; fila delantera: Lily Xi, Herbert Heyneker, Francisco Bolívar, Leonore Directo, Tadaki Hirose. Foto cedida amablemente por el City of Hope National Medical Center, Duarte, California.
Una vez con la experiencia y el financiamiento necesario, se inicia la carrera descrita por Hall, en la que participaron el grupo de Walter Gilbert en Harvard y la empresa Biogen, el grupo Rutter-Goodman en la Universidad de California, San Francisco (UCSF) y la empresa Eli Lilly, y el grupo también de la UCSF y el City of Hope National Medical Center, tanto con Genentech como Eli Lilly. La complejidad de la carrera queda de manifiesto con la presencia de dos grupos dentro de la misma universidad, la UCSF, además, ambos ligados con la misma empresa, Eli Lilly, la que como hemos visto inició y evolucionó a lo largo del siglo pasado asociada con la producción de insulina. Colaborando con estos grupos había desde luego un numeroso grupo de brillantes académicos, como Lydia-Villa-Komaroff, una investigadora de origen mexicano graduada en el MIT, quien en el grupo de W. Gilbert y empleando el pBR322 (Figura 7), logró expresar la proinsulina en E. coli (11). Una segunda opción de clonación consistía en la expresión de las dos cadenas que constituyen la insulina por separado y su posterior ensamblaje. A la larga, hacer un solo transgénico con el precursor de la molécula de insulina resultó más viable, por ser menos complejo y riesgoso.
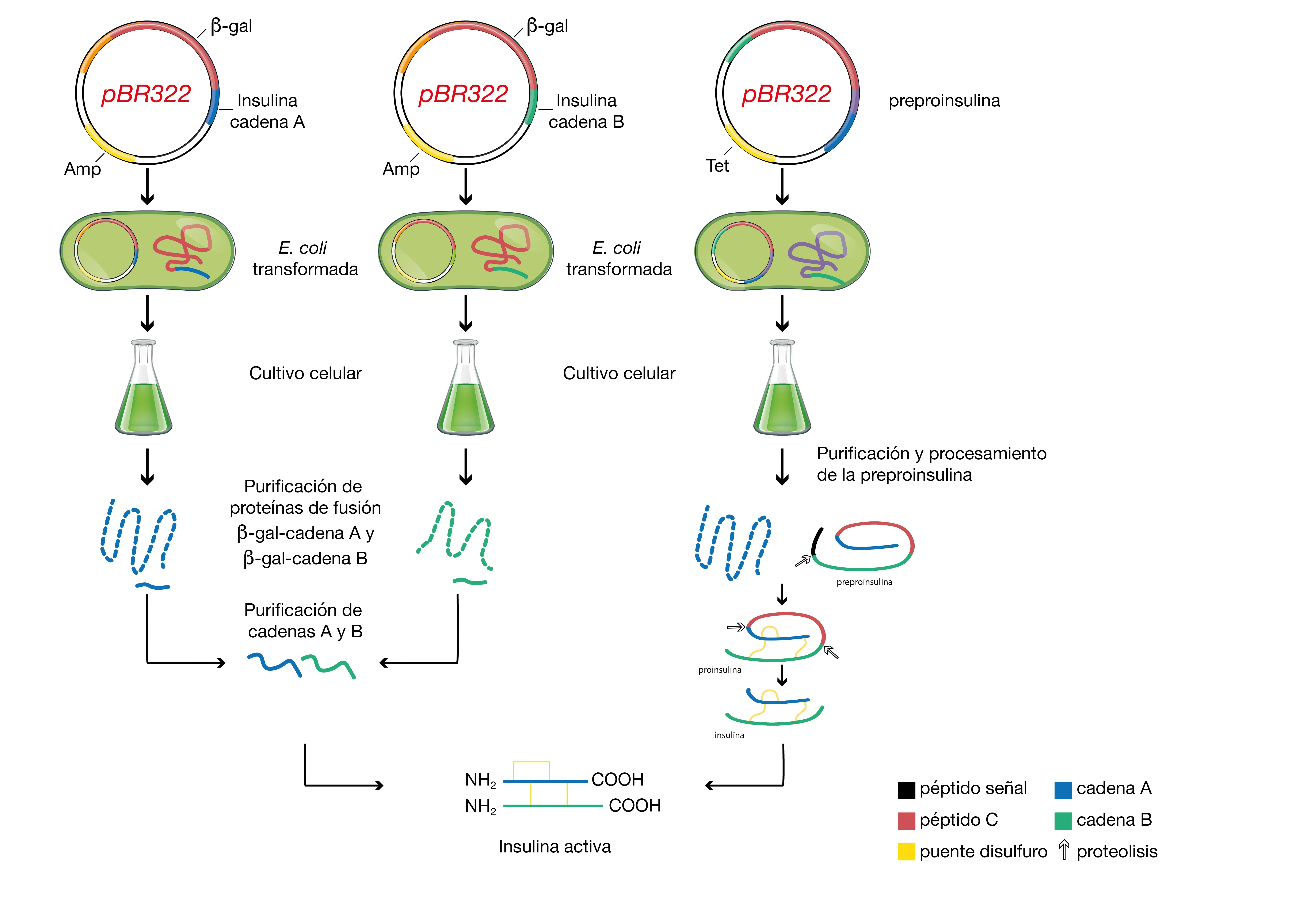
Figura 7. Esquema de las dos principales estrategias de ingeniería genética seguidas por los grupos que participaron en la búsqueda del proceso para la síntesis de insulina (ver figura X). A la izquierda la síntesis independiente de las cadenas A y B que la constituyen y su posterior ensamblaje; a la derecha, la síntesis de un precursor (preproinsulina) que contiene a la insulina integrada, ambas estrategias empleando el plásmido pBR3222 como vehículo molecular para transformar E. coli.
En los inicios de la década de los 80, con el conocimiento y herramientas desarrolladas en conjunto con el grupo de la UCSF, convencido de que la ciencia en México no podía quedar al margen de los avances en Biología Molecular, del conocimiento de la célula y del ADN, ni del aprovechamiento de sus poderosas herramientas, Francisco Bolívar, con un grupo de pioneros crearon el Centro de Investigación en Ingeniería Genética y Biotecnología, hoy Instituto de Biotecnología (IBt) en la UNAM (Figura 8).

Figura 8. Centro de Investigación sobre Ingeniería Genética y Biotecnología (CEINGEBI), ahora Instituto de Biotecnología de la UNAM.
Así, la etapa inicial de desarrollo de nuestra entidad académica está estrechamente ligada a este gran proyecto: la síntesis de insulina humana por medio de la síntesis de las dos cadenas por separado y su posterior ensamblaje. Por varios años un grupo de investigadores y estudiantes se encargaron de echar a andar diversas técnicas y de desarrollar conocimiento para aislar, secuenciar y sintetizar genes, para amplificarlos con la entonces incipiente técnica de la PCR (hoy popular por el diagnóstico del SARS-Cov2); aprendieron a analizar y purificar proteínas, así como a crecer células en fermentadores, todo esto hoy parte de las fortalezas del IBt-UNAM.
La esencia misma del esquema de trabajo “en grupos” que desde su creación priva en el IBt, se inspira en el proyecto de síntesis de insulina. Se trata de grupos en los que estudiantes, técnicos e investigadores colaboran alrededor de uno o dos líderes académicos, todos con el apoyo de unidades de infraestructura institucional (Figura 7). Esto representó un cambio de paradigma al esquema de trabajo académico en la UNAM, consecuencia de la necesidad de colaboración multidisciplinaria que exige la biotecnología, para lograr un trabajo de trascendencia tanto en el ámbito de la ciencia básica, como aplicada.
Es importante reflexionar en este aniversario, que con la insulina ya armada en el laboratorio, el grupo en México se enfrentó a la necesidad de apoyos financieros extraordinarios y experiencias técnicas y administrativas adicionales, tales como la caracterización inmunológica o la necesidad de elaborar y purificar preparaciones proteicas a gran escala libres de virus; la realización de pruebas clínicas y desde luego, acceder al ámbito comercial nacional y al financiamiento en un país con ausencia de dichas instancias, de criterios de regulación y de empresas interesadas en la biología molecular. Desafortunadamente, esa situación no es muy diferente a la que enfrentaron diversos grupos nacionales, incluido el IBt ante la opción de producir vacunas contra el Sars-Cov2 a base de proteínas recombinantes. Afortunadamente compañías como PROBIOMED, a pesar de innumerables obstáculos dentro y fuera del país ha logrado importantes logros en este sector.
Una reflexión final
Quienes en espacios como la revista Biotecnología en Movimiento promovemos la divulgación de la ciencia en general y de la Biotecnología en particular, insistimos siempre en la necesidad de la prevención y del uso racional y -decimos ahora-, sustentable del conocimiento. Moléculas casi milagrosas como la insulina requieren para hacer racional y sustentable el milagro, cumplir con un importante principio: estar ligadas al uso racional asociado con la prevención. Si bien la insulina llegó a la medicina moderna para evitar ceguera y amputaciones, indultando de la sentencia de muerte que pendía sobre quienes padecían diabetes, no se deben perder de vista las causas y asociación con el modo de vida y los hábitos alimentarios. La insulina es nuevamente una muestra de cómo la ciencia en general, y la biotecnología en particular nos rescata; la penicilina y la insulina desde el siglo pasado, las vacunas a ARNm y cientos ya de proteínas transgénicas en el presente. Sin embargo, debemos corregir el rumbo para evitar enfermedades que pueden prevenirse favoreciendo así que los recursos se canalicen al tratamiento de padecimientos de difícil prevención, como son los ligadas a la genética.
REFERENCIAS
- Miller, H. (2023). Happy 41st birthday, genetically-engineered insulin. Your approval by the FDA in 1982 took 5 months. How many years would it take now? Genetic Literacy Project Newsletter. Octubre 24, 2023.
- Alberto de Leiva, Eulalia Brugués, Alejandra de Leiva-Pérez. El descubrimiento de la insulina: continúan las controversias después de noventa años (The discovery of insulin: continued controversies after ninety years). Endocrinología y Nutrición. 58, 9, 449-456, Nov. 2011.
- Mallory Warner. O say can you see? Behind “The birth of Biotech”. 21, Oct. 2013; and Diane Wendt Two tons of pig parts: Making insulin in 1920. (1st Nov. 2013). Stories from the Museum. National Museum of American History. https://americanhistory.si.edu/blog
- Brian Buntz. https://www.drugdiscoverytrends.com/50-of-2022s-best-selling-pharmaceuticals/. April 2023.
- GF Cohen SN, Chang AC, Boyer HW, Helling RB. (1973). Construction of biologically functional bacterial plasmids in vitro. PNAS USA. 70 (11): 3240-4. DOI: 10.1073/pnas.70.11.3240.
- Goeddel DV, Kleid DG, Bolívar F., Heyneker HL, Yansura DG, Crea R, Hirose T, Kraszewsky A, Itakura K., Riggs AD. Expression in E.coli of chemically synthesized genes for human insulin. PNAS 76 , 1, 106-110, 1979
- Bolívar F, Rodríguez RL, Greene PJ, Betlach MC, Heyneker HL, Boyer HW, Crosa JH, Falkow S. (1977) Construction and characterization of new cloning vehicles. II. A multipurpose cloning system. Gene. 2(2):95-113. PMID: 344137. DOI: 10.1016/0378-1119(77)90000-2.
- Stephen S. Hall. Invisible Frontiers: the race to synthesize a Human Gene. Atlantic Monthly Pr, 1987. ISBN 10-0871131471.
- Arthur D. Riggs. Making, Cloning and the Expression of Humnan insulin Genes in Bacteria. The Path to Humulin. Endocrine Reviews, 2021, Vol. 42, No. 3, 374–380.
- K. Itakura, T. Hirose, R. Crea, A. D. Riggs, H. L. Heyneker, F. Bolivar, H. W. Boyer. (1977). Expression in Escherichia coli of a chemically synthesized gene for the hormone somatostatin. Science 198(4321):1056-63.
- Lydia Villa-Komaroff, Argiris Efstratiadis, Stephanie Broome, Peter Lomedico, Richard Tizard, Stephen P. Naber, William L. Chick, Walter Gilbert. (1978). A Bacterial clone synthesizing proinsulin. PNAS, 75, No. 8, pp. 3727-3731
Comparte este artículo en redes sociales

Acerca de los autores
El Dr. Agustín López Munguía es líder académico e investigador consolidado en el área de la biotecnología industrial, en particular en aspectos relacionados con procesos de producción y aplicación de enzimas en el sector alimentario y farmacéutico, en el Instituto de Biotecnología de la UNAM.
Contacto: agustin.lopez@ibt.unam.mx
AGRADECIMIENTOS: Con mi agradecimiento a la Dra. Paulina Balbás por comentarios e ideas para el manuscrito.